2019年,我校紧扣国家“双一流”与江苏高水平大学建设任务,聚焦中医药领域重大科学问题和关键共性技术问题为目标,多学科开展协同攻关,取得了一系列创新性研究成果,在Nature、JAMA 、Journal of Clinical Oncology、Nature Communications、PNAS等高影响力学术刊物发表论文9篇,学校整体科研水平及内涵建设质量显著提升。
1、谭仁祥教授科研团队的研究成果“Enzyme-catalysed [6+4] cycloadditions in the biosynthesis of natural products”于2019年3月13日发表在《Nature》上。该研究首次鉴定出能够催化[6+4]环加成反应的一类酶家族,这类酶的发现将进一步拓展了人们对周环反应酶的认识,为源于天然产物的生物合成和分子转化提供了新的途径。
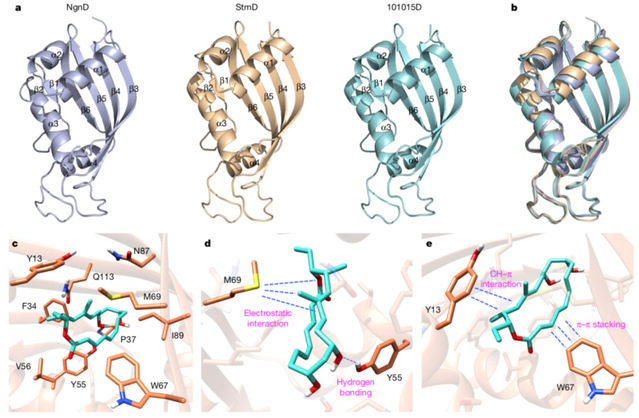
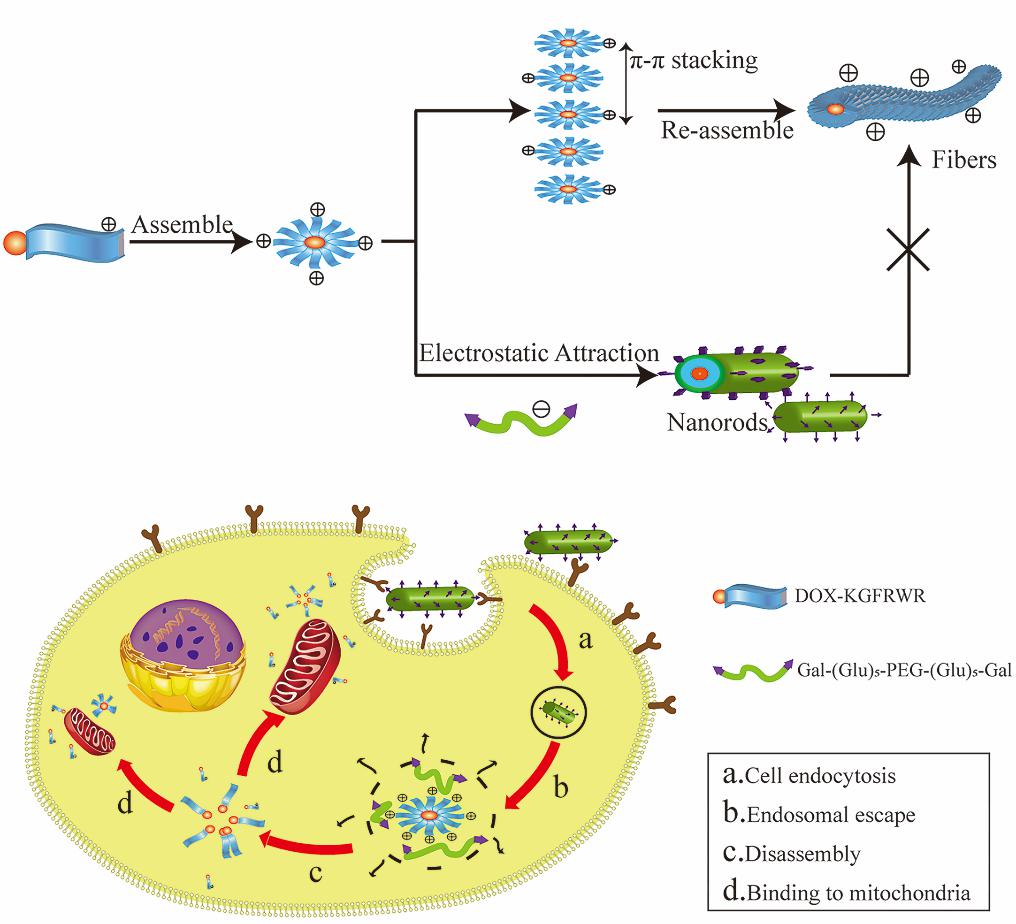
2、陈志鹏教授科研团队的研究成果“From Nanofibers to Nanorods: Nanostructure of Peptide-Drug Conjugates Regulated by Polypeptide-PEG Derivative and Enhanced Antitumor Effect”于2019年7月29日发表在《Advanced Functional Materials》上。该研究为基于多肽药物结合物构筑的多功能递释系统提供了新思路,该递释系统可促进纳米药物精准到达肿瘤部位而发挥治疗作用。
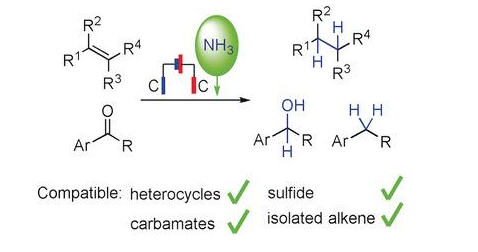
3、程旭教授科研团队的研究成果“Electrochemical Hydrogenation with Gaseous Ammonia”于2019年2月4日发表在《Angew Chem Int Ed Engl》上。该研究发现,使用氨作为氢源和碳电极对烯烃、炔烃和酮进行电化学加氢,能很好地耐受各种杂环和功能能性基团,为药物的电化学合成提供了一种新的途径。
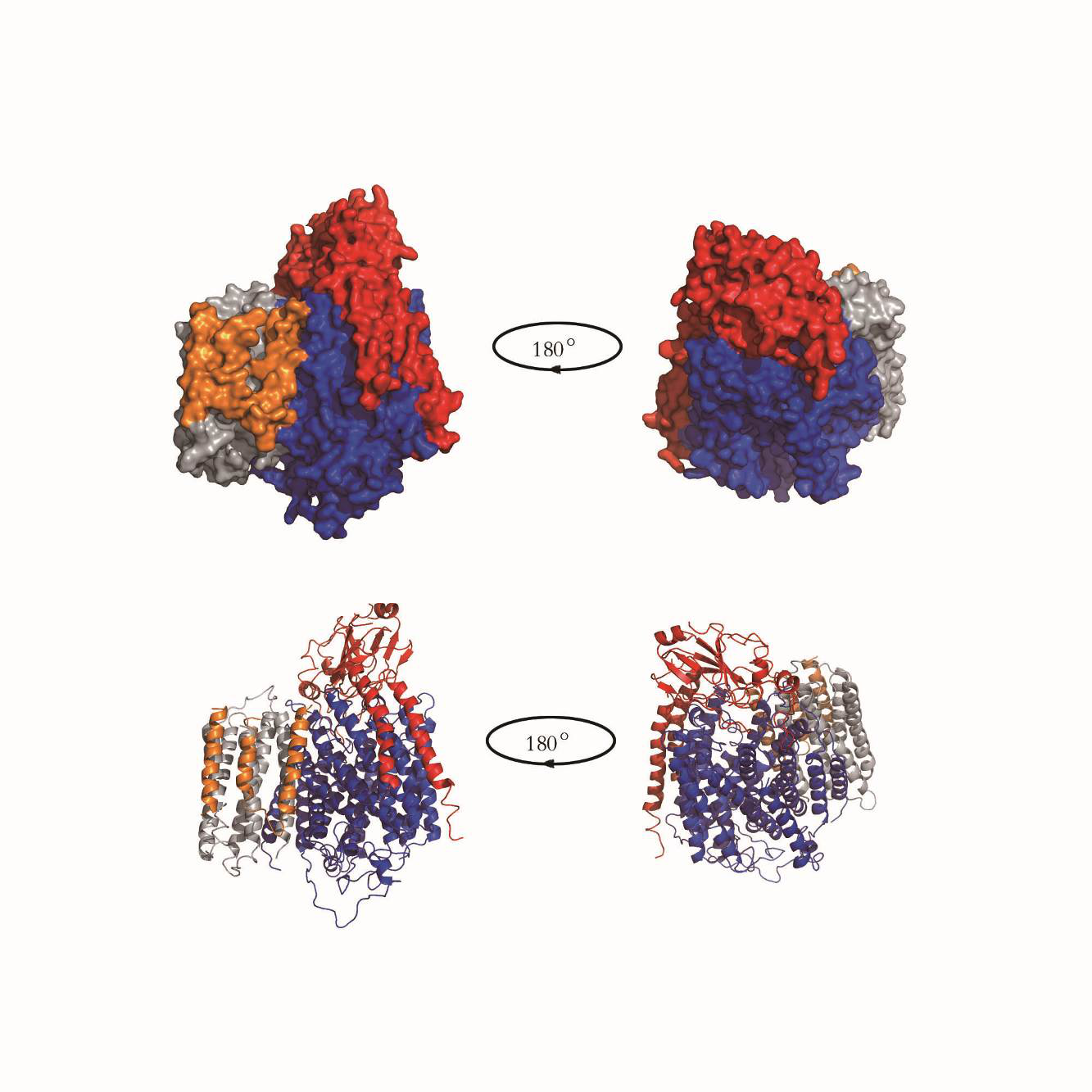
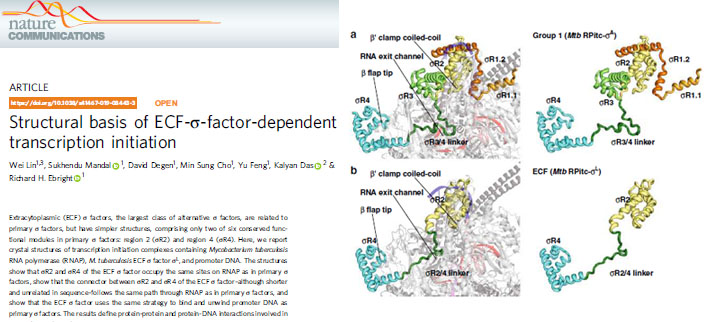
4、林炜教授科研团队的研究成果“Structural basis of ECF-σ-factor-dependent transcription initiation”于2019年2月12日发表在《Nature Communications》上。该研究解析了结核分枝杆菌 ECFs因子依赖型转录起始复合物的晶体结构,并回答了 ECFs因子如何通过与 DNA、RNA 聚合酶核心酶相互作用启动致病菌应激基因转录这一关键科学问题,为新型抗结核菌感染药物的开发提供新的思路。
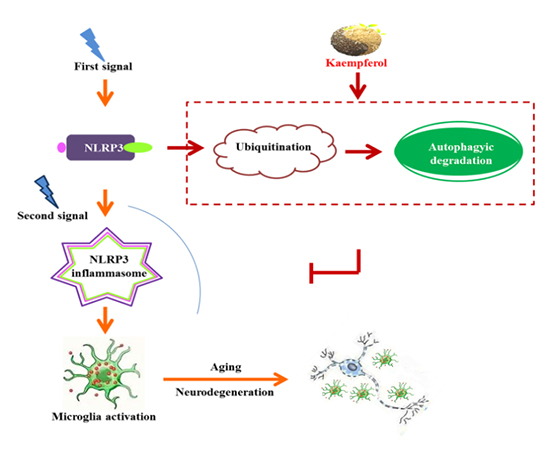
5、胡刚教授科研团队的研究成果“Small molecule-driven NLRP3 inflammation inhibition via interplay between ubiquitination and autophagy: implications for Parkinson disease”于2019年4月9日发表在《Autophagy》上。该研究揭示黄芪活性成分山奈酚(Kaempferol)通过抑制炎症小体活化介导的神经炎症,对帕金森病模型具有显著的神经保护作用,为基于天然产物研发新一代抗帕金森病药物提供了新思路。
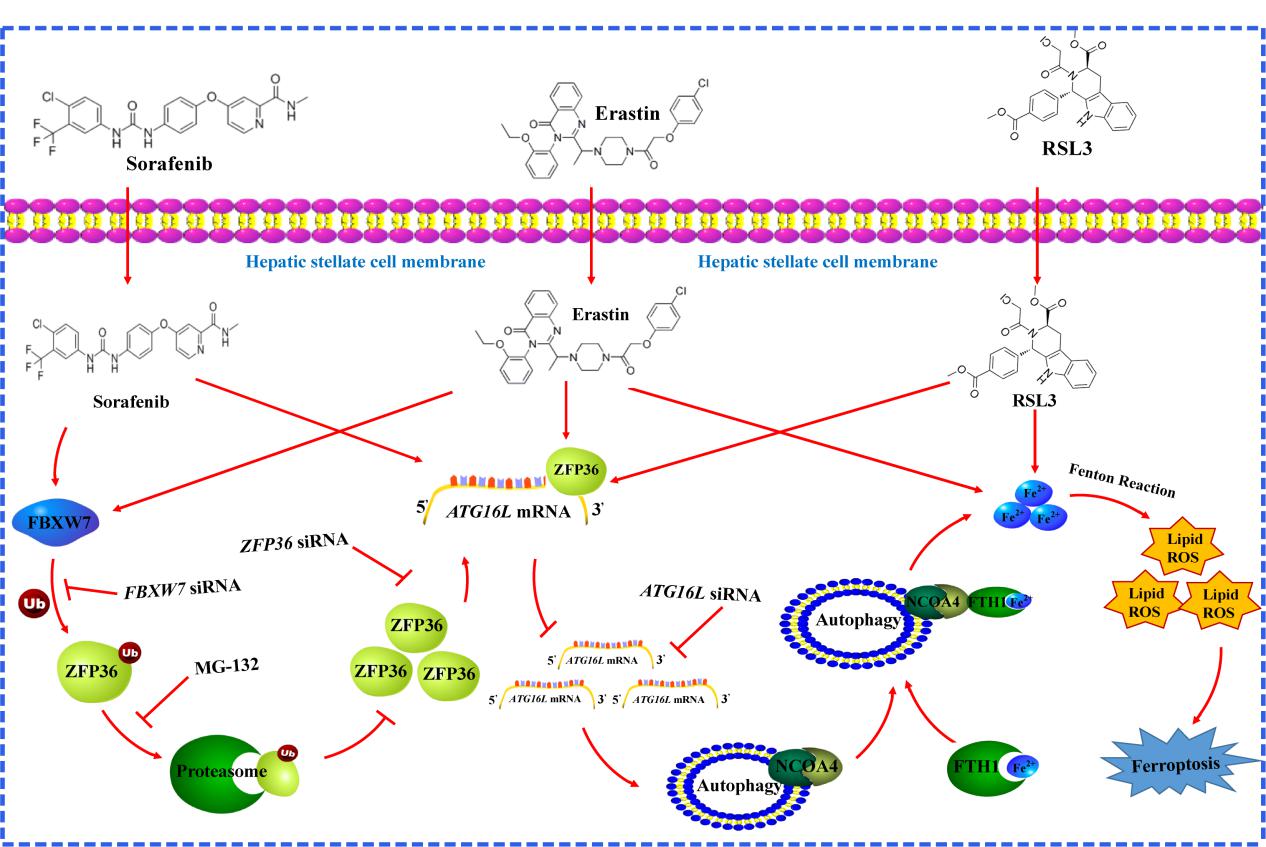
6、郑仕中教授科研团队的研究成果“RNA-binding protein ZFP36/TTP protects against ferroptosis by regulating autophagy signaling pathway in hepatic stellate cells” 于2019年11月11日发表在《Autophagy》上。该研究对RNA结合蛋白ZFP36在铁死亡的翻译后修饰中的作用提出了新见解,为进一步从转录后水平揭示铁死亡调控机制提供新的视角。
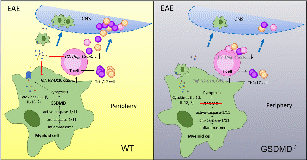
7、王冰微教授和胡刚教授科研团队的研究成果“Gasdermin D in peripheral myeloid cells drives neuroinflammation in experimental autoimmune encephalomyelitis”于2019年11月4日发表在《Journal of Experimental Medicine》上。该研究揭示了Gasdermin D在多发性硬化症发生、发展中的作用,提出了多发性硬化症免疫病理学的新见解,为基于GSDMD为靶点的多发性硬化症的临床治疗学和研发理想的治疗药物提供了学术基础。
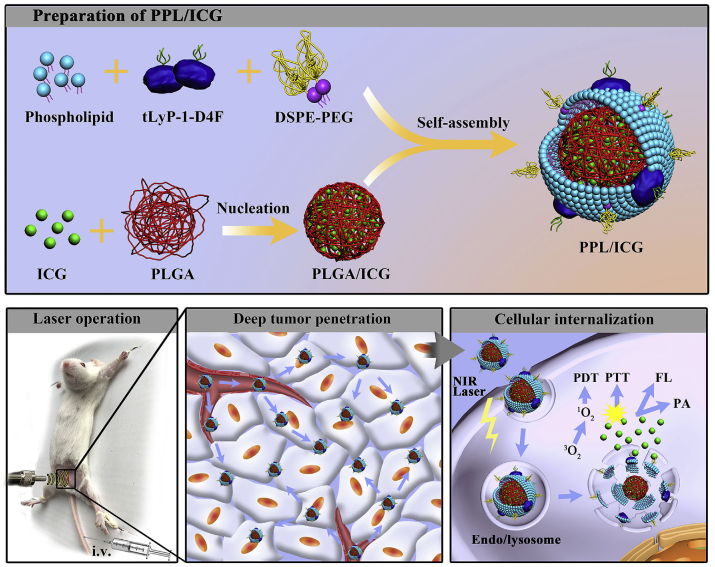
8、狄留庆教授科研团队的研究成果“Laser-triggered polymeric lipoproteins for precision tumor penetrating theranostics”于2019年11月发表在《Biomaterials》上。该研究为新型仿生诊疗平台的开发提供了实例论证,也为优化仿生型纳米药物载体提供新思路和新方法。
9、朱家鹏教授科研团队的研究成果“Structure of the Cytochrome aa3-600 Heme-copper Menaquinol Oxidase Bound to Inhibitor HQNO Shows TM0 Is Part of the Quinol Binding Site”于2019年12月发表在《Proc Natl Acad Sci USA》上。该研究解析了来源于枯草芽孢杆菌的Menaquinol Oxidase 3.6Å分辨率的蛋白晶体结构,揭示了此类酶的催化结构特征,为基于Quinol Oxidase的调节研发靶向性药物提供了重要的学术基础,。